КРОВОТЕЧЕНИЯ ПРИ ЦИРРОЗЕ ПЕЧЕНИ И ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ. НОВЕЙШИЕ МЕТОДИКИ ДИАГНОСТИКИ И ЛЕЧЕНИЯ.
Возможным этапом развития хронических гепатитов является формирование цирроза печени и синдрома портальной гипертензии. Кровотечение из вен пищевода является наиболее драматичным осложнением портальной гипертензии. В отсутствии квалифицированного лечения летальность превышает 70%, а иногда вообще не оставляет шансов на выживание.
Источники кровотечений портального генеза
В соответствии с анатомической локализацией источников кровотечения можно выделить пищеводные и желудочные геморрагии, а также кровотечения из «эктопических вариксов».
Основной механизм развития кровотечения портального генеза связан с повышением портального давления. Источник кровотечения может быть связан с разрывом относительно крупного венозного сосуда в подслизистом слое пищевода, что представляет собой наиболее частый вариант геморрагии.
Варикозное расширение вен пищевода
ВРВ пищевода являются наиболее частой причиной кровотечений. Высокая частота пищеводных кровотечений обусловлена анатомическими особенностями нижней трети пищевода (поверхностное расположение вен, повышение сосудистого сопротивления на этом уровне, наличие нескольких венозных уровней, соединенных коммуникантами).
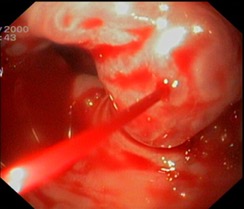
Эндоскопическая картина продолжающегося кровотечения из ВРВ пищевода
Варикозное расширение вен желудка
Проблемы эндоскопической диагностики варикозной трансформации желудочных вен связаны с их более глубоким расположением. ВРВ желудка могут являться как продолжением пищеводных вен, так и располагаться изолированно в своде желудка. Последний вариант чаще наблюдается при внепеченочном блоке.
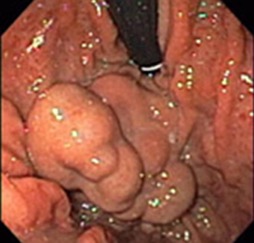
Эндоскопическая картина ВРВ свода желудка с использованием методики инверсионного осмотра
Несмотря на то, что факт выявления ВРВ желудка в целом не влияет на выживаемость пациентов, желудочное кровотечение является потенциально более опасным. Это обусловлено низкой лечебной эффективностью эндоскопических методов. Именно поэтому четкое клиническое разграничение пищеводных и желудочных кровотечений присутствует в большинстве современных лечебно-диагностических алгоритмов.
Эктопические вариксы
Эктопические вариксы — варикозное расширение вен в органах, кроме желудка и пищевода. Выявление эктопических вариксов чаще наблюдается при внепеченочной форме портальной гипертензии. Иногда их появление связывают с последствиями эндоскопической облитерации вен пищевода. Эктопические ВРВ встречаются преимущественно в желудочно-кишечном тракте.
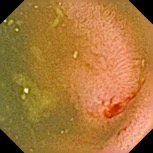
ВРВ тощей кишки (эктопический варикс),
диагностировано методом видеокапсульной эндоскопии
Эктопический варикс со стигмами состоявшего кровотечения
Кровотечение из эктопических варикозных вен — довольно редкое явление. Эта локализация варикозных вен является источником кровотечения приблизительно в 5 % случаев при внутрипеченочной портальной гипертензии и до 20 % при внепеченочной форме. Одна треть кровотечений из эктопических вариксов приходится на двенадцатиперстную кишку, одна треть — на тонкую кишку и одна треть — на ободочную кишку, из них 50 % — сигмовидная кишка.
Эндоскопическое лигирование
Быстрое и успешное внедрение метода лигирования ВРВ пищевода и желудка в программу профилактики и лечения варикозных кровотечений обусловлено рядом его преимуществ по сравнению со склеротерапией. Эндоскопическое лигирование быстрее позволяет достичь желаемого эффекта, более безопасно и легче переносится пациентами.
При остром кровотечении выполняют прямое лигирование кровоточащего участка варикозной вены.
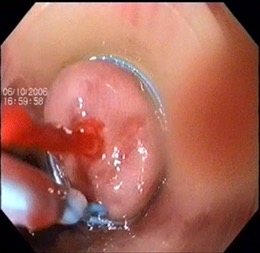
Методика прямого/прецизионного лигирования ВРВ пищевода
Для решения этой задачи эндоскоп подводят к зоне дефекта варикозной вены. Лигатура накладывается непосредственно на этот участок. В случае если не удается четко установить участок повреждения вены, проводится «спиральное» лигирование, когда эластичные кольца (лигатурные петли) накладываются последовательно по спирали на каждый варикозный ствол. На каждый ствол используют от 2 до 4 колец до полной остановки кровотечения.
Профилактическое лигирование изначально предполагает спиральный метод аппликации. Начиная от гастроэзофагеального перехода, лигатуры накладываются таким образом, чтобы в одной плоскости располагалась лишь одна лигатура. Соблюдение данной методики предотвращает развитие стенозов в пищеводе. Возможно наложение до 10 лигатур за один сеанс.
Облитерация варикозных вен тканевыми клеями
Эндоскопическая склеротерапия и лигирование не лишены целого ряда недостатков. В настоящее время используются преимущественно два цианакрилатных полимера: гистоакрил (n-бутил-2-цианакрилат) и букрилат (изобутил-1-цианакрилат). К особенностям тканевых клеев относится их замедленная полимеризация в физиологическом растворе в течение 20 сек. Введение гистоакрила в кровоточащий варикозный узел обеспечивает эффективную остановку кровотечения, так как образующийся полимер, приобретая в просвете сосуда твердую консистенцию в виде «слепка» вены, надежно прекращает в ней кровоток.
Из всех эндоскопических методов облитерация тканевыми клеями является технически наиболее сложной. При выполнении облитерации велика роль фактора времени в успехе лечения. Все манипуляции должны выполняться быстро, что требует специальной подготовки и взаимопонимания персонала.
Существуют рекомендации при проведении облитерирующего лечения смешивать гистоакрил с 0,5—0,8 мл масляного контрастного вещества липиодола с целью предупреждения быстрого затвердевания препарата и возможности последующего рентгенологического контроля.
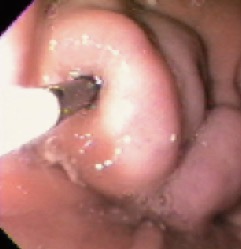
Методика интравазального введения склерозанта (гистакрил + липиодол)
Использование интравазального введения клеевых композиций позволяет добиться гемостаза в 90—100 % случаев. В связи с технической сложностью данного метода, которая определяется необходимостью обязательной четкой визуализацией источника геморрагии и строгого интравазального введения препарата, использование клеевых композиций при любом кровотечении из ВРВ пищевода и желудка нецелесообразно. Рационально использование цианакрилатов для остановки кровотечения из ВРВ желудка, когда стандартные склерозанты малоэффективны, при массивных кровотечениях из ВРВ пищевода, а также в случае ранних рецидивов кровотечений.
Самораскрывающийся металлический стент
В клинике был разработан модифицированный вариант — стент Элла-Дениша, который позволяет выполнить лечебную манипуляцию без рентгенологического или эндоскопического контроля. Стент Дениша сделан в форме, которая соответствует анатомической конфигурации пищевода и варикозно расширенных вен, особенно его дистальной части — 4—6 см. Длина стента — 135 мм.
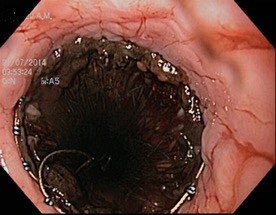
Стент Дениша в просвете пищевода (эндоскопический контроль и оценка эффективности установки)
При установке СМРС были выявлены следующие преимущества:
- стент не может быть удален или смещен самим пациентом в состоянии возбуждения;
- просвет стента обеспечивает физиологический дренаж слюны. Возможен прием жидкости и пищи через рот;
- тщательный повторный осмотр пищевода, кардии, желудка и 12-перстной кишки, а также эвакуация желудочного содержимого возможна сразу же после введения стента.
Установка стента для прекращения кровотечения из варикозно расширенных вен пищевода является инновационной методикой, которая была применена у пациентов в чрезвычайных ситуациях, связанных с высоким риском для жизни. Процедура не вызвала осложнений и привела к быстрой остановке кровотечения у всех больных. Конечно, необходимы дальнейшие исследования, чтобы подтвердить эти первоначальные положительные данные.
Хирургические вмешательства
По основной патогенетической направленности выделяют операции портосистемного шунтирования и портоазигального разобщения.
Снижение портального давления методом портосистемного шунтирования устраняет один из решающих патогенетических факторов возникновения кровотечений из ВРВ пищевода и желудка.
Бурное развитие хирургической техники и совершенствование анестезиологического обеспечения создали в начале 1940-х гг. предпосылки для развития операций портосистемного шунтирования. Применение сосудистых портосистемных шунтов в клинической практике выдвинуло целый ряд проблем. Операционная травма зачастую становится непереносимой для большинства декомпенсированных больных циррозом печени. Синдром портосистемной энцефалопатии усугублялся у большинства оперированных больных. В 1970-е гг. период увлечения декомпрессивными операциями сменился более сдержанным к ним отношением. Были обобщены отдаленные результаты, показывающие отсутствие увеличения продолжительности жизни пациентов после операций портосистемного шунтирования. Стало очевидным фактом, что портальная декомпрессия приводит к снижению функциональных резервов печени, увеличению частоты развития и тяжести течения портосистемной энцефалопатии.
После портосистемного шунтирования снижаются процессы регенерации печени. В выборе типа шунта существуют своеобразные «ножницы»: чем больше диаметр шунта, тем выраженнее декомпрессивный эффект вмешательства, но при этом выше послеоперационная летальность, чаще возникает энцефалопатия, меньше продолжительность и ниже качество жизни пациентов. И наоборот, малый диаметр шунта сопровождается меньшей летальностью, энцефалопатией, умеренным угнетением печеночной регенерации, но при этом часто оказывается неэффективным в снижении портального давления. Ряд исследователей находят, что практически любой тип сосудистых портосистемных анастомозов способствует прогрессированию дистрофических процессов в печени и часто осложняется развитием печеночной энцефалопатии. Главный недостаток портосистемных анастомозов связан с существенным снижением портальной перфузии печени и увеличением объема шунтирующейся крови.
В настоящее время больше внимание уделяется не селективности шунтирования, а степени портальной декомпрессии. Доминирующую позицию занимает концепция парциальной (дозированной, частичной) портальной декомпрессии. Оптимальным считается диаметр анастомоза 6—8 мм. При этом существенно снижается риск кровотечения, а снижение функции печени и усугубление портосистемной энцефалопатии не выражены.
Процедура чрезъяремного внутрипеченочного портосистемного шунтирования является одной из последних новаторских технологий, позволяющей выполнить эффективную декомпрессию портальной системы. В англоязычной научной литературе для обозначения этого вмешательства общепринято использовать аббревиатуру TIPS — Transjugular intrahepatic portosystemic shunt.
Идея создания портальной декомпрессии путем чрескожного формирования внутрипеченочного соустья между крупными печеночными и воротной венами впервые была сформулирована и осуществлена в эксперименте Josef Rosch (1969). Разработка компактных металлических сосудистых эндопротезов в конце 80-х гг. позволила вывести процедуру TIPS на клиническую сцену и обеспечила техническую основу успешного формирования венозно-венозной фистулы в паренхиме печени. Первое клиническое использование процедуры было выполнено G. Richter [et al.] (1990). Начиная с этого времени, началось повсеместное внедрение методики TIPS в клиническую практику.
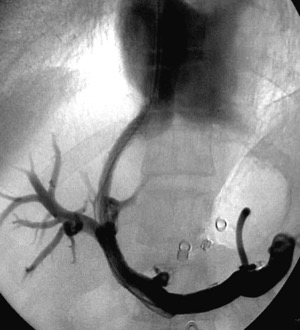
Процедура внутрипеченочного портоситемного шунтирования
«Технический успех» TIPS (т. е. успешное вмешательство и выживаемость пациентов в течение 30 дней) достигает высоких значений и составляет 93—100 %. Отсутствие рецидива кровотечения в течение 1 мес. наблюдается в 83 % случаев. Наибольшее число осложнений отмечается среди пациентов Child С и при наличии асцита, свидетельствующего о декомпенсированной функции печени.